1.1.3 配位化学理论
配位化学讨论配合物化学键的基本理论模型主要有价键理论、晶体场理论和分子轨道理论。
价键理论是将杂化轨道理论和电子对成键概念应用于配合物中,在20世纪30年代,由L.Pauling将杂化轨道理论应用于配合物的研究,并且用该理论比较恰当的解释了一些配合物的结构和性质[6-7]。至此之后的20年里,人们都主要用这种理论来讨论配合物的化学键,由此,配合物的价键理论逐渐成熟。价键理论主要阐述了三个方面的内容:第一,在配合物形成时由配体提供的孤对电子进入形成体的空的价键电子轨道而形成配键;第二,为了形成结构均匀的配合物,主要采取杂化轨道与配体形成配位键;第三,不同的杂化轨道有不同的空间结构[8]。虽然该理论在如今已经很少用,但是讨论配位键时任然会使用杂化轨道理论。
在价键理论提出的同时,H. Bethe 和J. H. Van Vleck在三十年代初提出了晶体场理论。该理论在20世纪50年代取代了价键理论,被广泛的应用于配合物化学键的问题中。它与价键理论的区别在于它将中心离子与配体看做点电荷,当形成配合物时,中心离子与配体异性相吸,而配体之间同性相斥。它也考虑了,带负电荷的配体对于中心离子最外层电子的排斥作用。这种排斥作用所形成的静电场被称为晶体场。晶体场理论的主要观点有:第一,中心离子与带负电的配体完全是依靠静电作用结合在一起,由此形成的配合物才有稳定性;第二,配体形成的晶体场对中心离子的电子(尤其是d轨道电子)产生排斥作用,使轨道能及分裂,有些轨道能级升高,有些则降低;第三,在结构不同的配合物中,所形成的不同的晶体场对于中心离子d轨道的影响不同。各种晶体场下,d轨道分裂如图1.1所示。
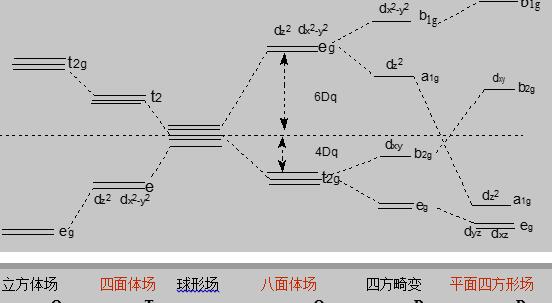
图1.1 各种晶体场下d轨道分裂图
随着检测技术的发展,通过核磁共振、X-射线粉末衍射、质谱分析等研究手段,使得人们能从微观的角度研究物质结构[9]。通过这些分析,人们发现中心离子与配体之间存在着轨道的重叠作用。运用晶体场理论的模型解释此类化合物会存在缺陷,这时应使用分子轨道理论。与晶体场理论不同,它考虑到了轨道的重叠与共价键的形成,与共价键理论不同,它考虑到了中心离子的原子轨道与配体轨道组成离域分子轨道,配离子的价电子不会单纯的在中心离子的轨道上或者配体轨道上运动,而是在整个离域轨道中运动。其基本理论要点如下:第一,在形成配合物时,所有的配体轨道通过线性组合形成配体轨道群,中心离子的轨道与该轨道进行对称性匹配形成新的分子轨道。分子轨道的能级图可通过解薛定谔方程得到。第二,电子在轨道中的排布遵循Pauli不相容原理和洪特规则(一个分子轨道中只允许两个自旋方向相反的电子存在,不可能出现两个自旋方向相同的电子;电子进入分子轨道时,优先考虑占据空轨道然后考虑成键。)。第三,中心离子与配体所形成的键键能不同,有σ键与π键。虽然分子轨道理论涵盖比较全面,但是它的计算过程是十分复杂且费时的 四齿配体的合成以及其Fe(II)配合物的构筑和表征(3):http://www.youerw.com/huaxue/lunwen_31354.html

